「wt%って聞いたことあるけど、よくわからない…」そんな方もご安心を♪
wt%(重量パーセント)は、成分がどれくらい含まれているかを表すとても身近な指標なんです。
たとえば、ジュースの果汁やスキンケアの成分表示、さらには理科の実験や工業製品の配合比率まで、意外といろんなところで活躍しています。
この記事では、wt%の意味・計算方法・他の濃度表示(mol%、ppmなど)との違いから、実際の測り方や覚え方のコツまで、やさしい言葉でていねいにご紹介します♪
理系が苦手な方でも大丈夫!一緒にwt%の世界をのぞいてみましょう。
wt%(重量パーセント)とは?

wt%の定義とシンプルな言い換え
wt%とは「weight percent(重量パーセント)」の略で、ある成分が全体の重さの中で何パーセントを占めているかを表す単位です。たとえば、100gの食塩水に5gの食塩が含まれていれば、食塩のwt%は5%になります。
このように、wt%は「どのくらいの割合で含まれているか」を示す、とても基本的な考え方です。特に化学や理科の学習では必ず登場する単位であり、「割合の感覚を身につける」のにぴったりな入り口ともいえるでしょう。
濃度表示としてのwt%の役割
wt%は、液体の濃度や材料の配合比を示すのによく使われます。たとえば化粧水の成分表示や食品の栄養成分表示、さらには工業用の洗浄液の濃度管理など、実にさまざまなシーンでwt%が使われているんです。
他にも、洗剤・漂白剤・アルコール消毒液のような「何がどれくらい含まれているか」が重要な製品では、wt%での濃度表記が基本になります。重さを基準とすることで、正確で安定した品質管理ができるのも大きなメリットです。
食塩水・飲料など身近な例でイメージしよう
・5gの塩を95gの水に溶かした→wt%は5%
・100gのジュースに果汁10g→果汁wt%は10%
・50gのチョコレートにカカオマスが25g含まれていれば→wt%は50%
このように、wt%の考え方は、家庭でも使えるとても実用的なものなんです。料理や掃除、スキンケア用品を選ぶときにも「成分の割合」を見るときに、wt%の知識は役立ちますよ。
「身近にある例でイメージする」ことで、wt%がぐっと親しみやすくなります。
wt%の計算方法|初心者向けにやさしく解説
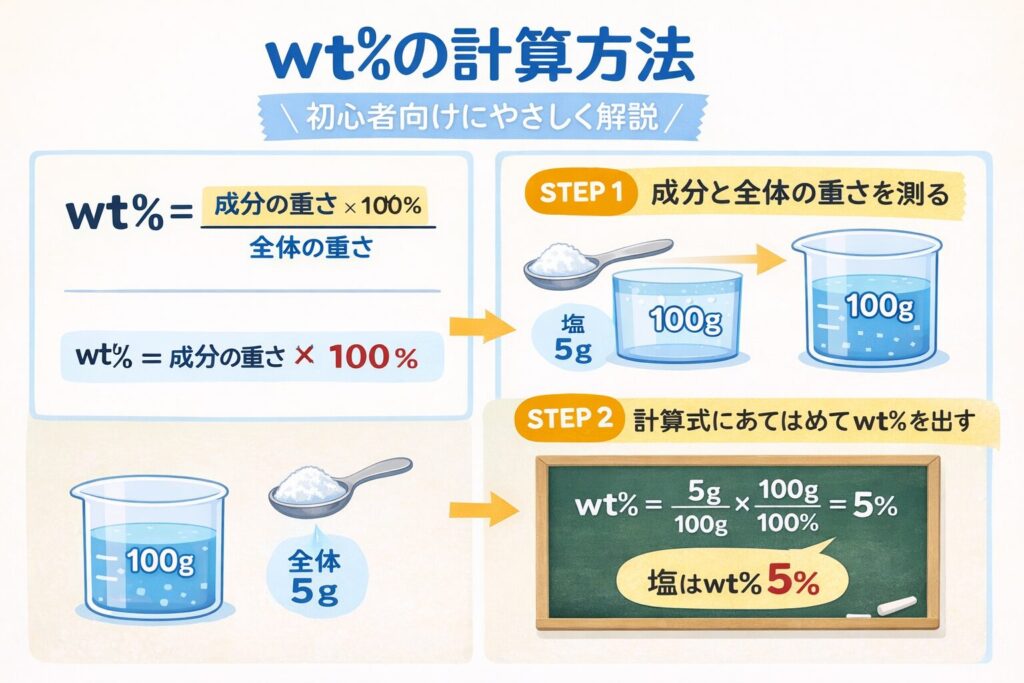
wt%の基本計算式
wt% =(成分の重さ ÷ 全体の重さ)× 100
例:5gの塩 ÷ 100gの食塩水 × 100 = 5%
この計算式は非常にシンプルですが、「重さでの割合」だという点が重要なポイントです。「体積」や「モル数」ではなく、「重さ」だけに注目するのがwt%の特徴です。
たとえば、100gの液体の中に成分が5g含まれていたら、それはwt%で5%という意味になります。逆に言えば、「全体の重さに対して成分がどれくらい含まれているか」を把握できれば、簡単にwt%は求められるんですね。
例題で学ぶ!食塩水・洗剤などでステップ解説
【例題1】
Q:3gの洗剤を97gの水に溶かしました。wt%は?
A:(3 ÷(3+97))×100 = 3%
→合計100gの中で3gが洗剤なので、wt%は3%になります。
【例題2】
Q:2gの塩を198gの水に溶かすと?
A:(2 ÷(2+198))×100 = 1%
→このように、数値を変えても同じ手順で計算できます。
【例題3】
Q:5gのクエン酸を45gの水に入れたら?
A:(5 ÷(5+45))×100 = 約10%
これらのステップを通して、どんな液体でも「重さ」さえ分かれば、wt%はすぐに出せることがわかります。
よくある計算ミスと注意すべき落とし穴
・「成分量÷全体量」で計算することを忘れずに!
・全体の重さ=成分+水(または溶媒)をきちんと足すこと!
・計算機で「×100」を忘れて小数のまま答えてしまうことも多いので注意しましょう。
また、「体積」での割合と勘違いしてしまう人もいますが、wt%はあくまで“重さ”が基準。体積と密度が関係するvol%やmol%とは別の概念なので、混同しないようにしてくださいね。
【保存版】wt%計算ドリル(例題つき)
初心者の方でも楽しく学べるように、いろいろなパターンの例題を用意しました。実生活でも使えそうなシチュエーションをイメージしながら、ぜひ一緒にチャレンジしてみてくださいね♪
例題①:100gの水に5gの塩 → wt%は?
(5 ÷ 105)×100 = 約4.76%
→水と塩の合計は105g。そのうち塩が5gなので、重さの割合は約4.76%になります。料理の塩分計算にも応用できます。
例題②:wt%3%の液を200g作るには何g必要?
200 × 0.03 = 6g(成分量)
→3%濃度で200gの液を作るには、成分(たとえば洗剤や薬品)を6g加えればOK。残りの194gは水などの溶媒という計算になります。
例題③:wt%と成分量から全体量を求める方法
Q:wt%が4%で、成分が8gのとき、全体の重さは?
→ 8 ÷ 0.04 = 200g
→このように、濃度と成分量のどちらかがわかれば、逆算で全体の重さも計算できます。とっても便利ですね♪
例題④:150gのローションにグリセリンを5%加えるには何g必要?
150 × 0.05 = 7.5g
→5%濃度にしたい場合は、グリセリンを7.5g加えることで完成します。
例題⑤:合計300gの液体に成分が12g含まれています。wt%は?
(12 ÷ 300)×100 = 4%
→食品表示や化粧品などで「全体の中にどれくらい含まれているか」を計算するときに役立ちます。
計算の手順を身につけることで、日常の中でも「この濃度って何%かな?」と自然に考えられるようになりますよ♪
mol%、vol%、ppmとの違いって?

wt%・mol%・vol%・ppmの比較表と特徴
以下の表に、よく使われる濃度表記の違いをまとめました。それぞれの単位が「何を基準にしているのか(重さ・体積・粒子の数など)」を理解することが、正しく使い分ける第一歩です。
| 単位 | 意味 | 使われ方の例 |
|---|---|---|
| wt% | 重さの割合 | 食塩水・洗剤・化粧品の成分表示 |
| mol% | 分子の割合 | 化学反応式・電池材料・合成実験など |
| vol% | 体積の割合 | アルコール飲料・香料・ガス混合物 |
| ppm | 100万分の1の割合 | 大気汚染・水質検査・農薬濃度など |
たとえば、「お酒のアルコール度数○%」はvol%(体積%)ですが、「漂白剤の濃度○%」は通常wt%(重量%)です。ppmはごく微量な成分を表すのに便利で、水道水の塩素濃度や大気中の二酸化炭素量の表示にも使われます。
なぜwt%がよく使われるのか?
wt%は「重さ」を基準とするので、測定がとても簡単で再現性が高いという特徴があります。料理や洗剤、化粧品など、家庭での用途にもぴったりなんです。
さらに、実験や工業の現場では、体積よりも「質量の正確さ」が求められるため、wt%が採用されることが多くなっています。温度や圧力によって体積は変化しますが、質量は変わらないため、安定した管理ができるというメリットもあるんですよ。
変換はできる?密度との関係と注意点
mol%やvol%をwt%に変換するには、物質の密度や分子量などの情報が必要になります。
たとえば、
- vol%(体積%)→wt%(重量%):密度をかけて計算
- mol%(モル%)→wt%:分子量を使って換算
しかし、初心者の方が無理に変換しようとすると混乱しやすいので、最初のうちは「どの単位がどんなシーンで使われるか」を理解しておくのが大切です。
どの単位も一長一短がありますが、「場面に応じた選び方」を知っておくことで、濃度の読み取りや説明がグッとやさしくなりますよ♪
wt%の測定方法と実際の手順
測定に使う機器と準備
wt%を正確に測定するには、以下のような基本的な器具があると便利です。
- 電子天秤:できるだけ0.01g単位まで測れる精密なタイプがおすすめです。化学実験や調合の場面では、微小な差が結果に影響することもあるため、精度は大切です。
- 計量カップやビーカー:液体の体積ではなく、成分の「重さ」を正確に量るために、ビーカーや耐薬品性の容器があると安心です。
- スプーンやヘラなどの計量補助器具:成分をこぼさずに移すために使用します。
- 記録用紙や濃度表:測定結果を記録して比較や調整に役立てるために用意しておくとよいでしょう。
最近では、家庭用のデジタルスケールでも十分な精度を持ったものがあります。料理や手作りコスメなど、日常使いにも応用できます。
測定の流れと手順(学校・実験室の事例)
- 容器の重さを確認(風袋引き):最初に容器だけの重さを量り、差し引くことで正確な成分の重さを得られます。
- 成分の重さを量る:添加する成分(例:塩や薬品など)の重さを測ります。
- 全体の重さを量る:成分を容器に入れた後、水や溶媒を加えて全体の重さを計測します。
- wt%を計算式にあてはめる: wt% =(成分の重さ ÷ 全体の重さ)×100
- 記録と確認:計算結果を記録し、目的の濃度と一致しているか確認します。
このような基本の流れを覚えておくと、自分でいろいろな液体の濃度を調整したり、チェックしたりすることができます。
初心者にもおすすめ!簡単に使える測定アイテム紹介
最近では、家庭向けの精密なスケールや濃度チェッカーも手軽に入手できるようになっています。
- デジタルスケール(0.01g単位):キッチン用品コーナーやネット通販で購入できます。小型で収納もしやすく、料理・実験・手作りコスメなど幅広く活用できます。
- ハンディ濃度計:飲料の糖度や塩分濃度を測るタイプが人気。透明な液体に特に向いています。
- pHメーターや温度計との併用もおすすめ:濃度以外の環境条件も合わせて測れると、より高精度なコントロールが可能になります。
楽天やAmazonなどで「電子スケール 濃度計」と検索すると、用途や予算に応じたさまざまな商品が見つかりますよ♪
wt%が使われる主な分野とは?
中学・高校の理科実験(食塩水・酸・アルカリ)
wt%は、学生の理科教育の現場で基礎的な知識として登場します。特に、食塩水の濃度計算や中和反応の実験、酸やアルカリの希釈などの単元でよく使われます。生徒が「濃度ってどうやって計算するの?」と学ぶ第一歩として、wt%はとても重要な役割を果たしています。
また、文化祭の準備や化学部の活動でもwt%を活用する場面があり、自分たちで洗剤や香水などを作る際にも、「どれだけの成分を混ぜるとちょうどよくなるか?」という計算に使われています。こうした実体験を通じて、wt%は「数字の中の生活実感」として身につくことが多いのです。
食品・飲料業界(糖分・塩分表示)
食品表示を見たときに、「ナトリウム0.2g(食塩相当量0.5g)」や「たんぱく質5g」といった記載がありますが、これらは多くの場合、wt%に基づいて計算された情報です。
例えば、「このジュースには果汁が10%含まれています」といった表示の“%”もwt%であり、成分が全体の重さに対してどのくらいあるのかを示しています。また、濃縮還元ジュースや栄養ドリンクなど、配合が厳密に管理されている製品では、wt%による調整が欠かせません。
さらに、栄養バランスや糖質制限を意識する現代では、wt%は「何をどれだけ摂取しているか」を知る大事な手がかりにもなります。
医療・薬品・工業分野(点滴、洗浄液、溶剤など)
医療現場では、点滴や注射液などの濃度管理においてwt%は不可欠な単位です。たとえば「生理食塩水(0.9% NaCl)」という表示は、100gの水溶液に0.9gの塩化ナトリウムが溶けていることを意味します。
また、製薬業界でも薬剤の調合や濃度設定にはwt%が基準となり、患者の体重や状態に応じた正確な投与が必要です。そのため、ほんのわずかな誤差でも効果や副作用に関わることから、wt%の計算は非常にシビアに行われます。
さらに工業の分野では、洗浄液、冷却液、塗料、金属加工液などの成分比率の調整にwt%が用いられています。大規模な製造ラインにおいては、品質を安定させるためにもwt%は欠かせない基準となっています。
初心者Q&A|wt%の疑問を解消しよう
「wt%の%は単位?記号?」
この「%(パーセント)」は、実は単位というより“割合”を表す記号です。英語で「percent」と書き、「per(〜あたり)」と「cent(100)」が組み合わさった言葉。
つまり「%」は「100分のいくつか」という意味になります。たとえば「wt%=5%」なら、「全体100gのうち5gがその成分ですよ」ということなんですね。
科学の世界では「%」はとてもよく使われる記号で、数字の後ろにこの記号がついていることで“割合の比較”や“濃度”を一目で示すことができます。
「気温や湿度でwt%は変わるの?」
wt%は“重さ”を基準にした割合なので、基本的に温度や湿度の影響をあまり受けません。
たとえば、体積(ml)での表示は、温度が上がると膨張して増えて見えることがあります。でも重さ(g)は、ちょっと気温が上がったくらいではほとんど変わりませんよね。
このため、wt%は「安定性が高い」というメリットがあります。温度管理が難しい環境でも、濃度の表記や計算を一定の基準で行えるため、実験や工業、医療の現場で好まれるんです。
ただし、極端に湿度が高いと、粉末や吸湿性の高い成分が水分を含んでしまい、正確なwt%が出にくくなるケースもあるため、乾燥保存や風袋引きの徹底が大切になります。
「mol/Lとの違いがよくわかりません…」
とってもよくある疑問です!
- wt%(重量パーセント):重さを基準にした濃度(何g入ってる?)
- mol/L(モル濃度):物質の“粒の数”を基準にした濃度(何個分の粒が入ってる?)
つまり、wt%は「どれだけの重さで混ざってるか」、mol/Lは「どれだけの分子やイオンが溶けているか」を表すんですね。
理科や化学では、反応式を扱うときにmol/Lが重宝されますが、日常的な製品表示や家庭用にはwt%のほうがわかりやすく、使いやすいです。
イメージ例:
- wt% → お料理で「砂糖を20g入れる」
- mol/L → 実験で「HClを0.1mol/Lに希釈する」
それぞれの単位に向き・不向きがあるので、「使う場面に応じて選ぶこと」が大切です♪
wt%をやさしく覚えるコツ
「全体の中にどれくらい?」で考えると簡単
wt%の基本は、「全体100gの中に、何gの成分が含まれているか?」というシンプルな割合の考え方です。
たとえば、100gの液体の中に5gの塩が溶けていたら、それはwt%で5%。このように、“100gあったらそのうち何gが成分か”をイメージできれば、自然とwt%の感覚がつかめてきます。
このとき、「体積」や「モル」などの難しい単位は一旦忘れて、“重さだけ”に集中すると理解しやすいですよ。
お弁当や化粧品で例えるとわかりやすい
数字が苦手な方は、身近なもので例えるともっと理解しやすくなります。
たとえば、100gのお弁当の中に唐揚げが10g入っていたら、その唐揚げのwt%は10%になります。化粧品でいえば、「100gのクリームにヒアルロン酸が1g含まれていたら、wt%は1%」という計算です。
他にも…
- 100gのシャンプーに香料が2g → wt%は2%
- 200gのジュースに果汁が30g → wt%は15%
このように、日常の“量と割合”を意識するだけで、wt%が一気に身近になります。
「100gのうち何g?」を数字でイメージする習慣
感覚だけで「多い」「少ない」と判断するよりも、実際に数字で考えるクセをつけると、濃度の違いが明確にわかるようになります。
たとえば、
- 100g中に1g → 1%(かなり薄め)
- 100g中に10g → 10%(標準的)
- 100g中に30g → 30%(濃いめ)
この“数字の感覚”が身につくと、商品ラベルを見たときに「これは成分が多いな」「思ったより薄めかも」と判断できるようになりますよ。
最初は電卓を使ってもOKです。慣れてきたら、頭の中でざっくり計算できるようになると、日常生活でもとっても役立ちます♪
まとめ|wt%を使いこなせば濃度の仕組みがわかる!
wt%は「全体に対して、成分が何g入っているか」を示すシンプルで直感的な指標です。「難しそう…」と思われがちですが、実はとても身近で使いやすい考え方なんです。
食品のラベルを見たり、スキンケア商品の成分をチェックしたり、理科の授業や趣味の調合・DIYでも、wt%の考え方が役立ちます。数字で「どれくらい含まれているか」がわかると、選ぶ・比べる・調整するといった行動にも自信が持てるようになりますよ。
また、mol%やppmとの違いをおさえて、場面に応じた濃度表記を選べるようになると、理科の理解や実験精度がグッとアップします。重さを基準にしているwt%は、温度や体積の影響を受けにくく、誰でも扱いやすいというメリットも大きいです。
まずは、「100gの中に何g入ってるのかな?」という感覚を持つことから始めてみましょう。数字が味方になると、暮らしも勉強ももっと楽しくなりますよ♪


